2023年3月15日,华中科技大学生命学院、国家纳米药物工程技术研究中心李子福教授、杨祥良教授团队在国际权威期刊Nature Communications上发表题为“Mechano-boosting nanomedicine antitumour efficacy by blocking the reticuloendothelial system with stiff nanogels”的研究论文。
纳米药物已经广泛应用于肿瘤临床治疗,但是网状内皮系统的快速清除严重限制了其治疗效果。网状内皮系统阻塞(RES-blockade)策略可以暂时性地、可逆地延缓肝脏清除,提高纳米药物的肿瘤富集以及抗肿瘤作用,具有良好的生物安全性。然而,循环系统中大量的纳米颗粒仍然会对网状内皮系统带来额外的负担,因此提高RES-blockade策略效率尤为重要。研究表明,RES-blockade策略的效率受到多种因素的影响,包括阻塞与给药的时间间隔、阻塞剂量以及阻塞材料的理化性质等。纳米颗粒的力学性能显著影响纳米药物体内递送的五个关键过程,包括血液循环、肿瘤富集、深部穿透、细胞摄取以及药物释放,然而对RES-blockade策略效率以及巨噬细胞功能的影响尚不清楚。
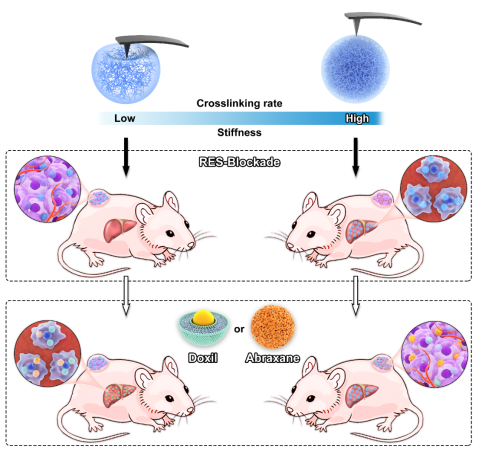
图1. 力学赋能纳米药物抗肿瘤作用策略示意图
针对以上研究现状,本工作设计了一系列具有不同硬度的纳米凝胶,探究如何利用纳米凝胶的力学性能克服网状内皮系统的清除作用;并提出了力学赋能抗肿瘤作用的治疗策略,结合硬质纳米凝胶在阻塞网状内皮系统中的高效性以及软质纳米凝胶在药物递送过程中的优势,使抗肿瘤作用最大化,即“硬阻软输”策略(图1)。在本策略中,优先注射硬质纳米凝胶,通过抑制网格蛋白介导的细胞内吞途径以及在肝脏部位的滞留效应,抑制巨噬细胞的摄取能力并暂时性地阻塞网状内皮系统。随后,注射搭载盐酸阿霉素的软质纳米凝胶,凭借优异的变形能力克服肿瘤致密的细胞外基质,实现更高的肿瘤富集量、更深的肿瘤组织穿透以及更高效的抗肿瘤作用。综合利用不同力学性能的纳米凝胶在药物递送各个阶段的优势,实现最佳的抗肿瘤效果。同时,基于硬质纳米凝胶的RES-blockade策略对于上市纳米药物,如Doxil和Abraxane的抗肿瘤效果同样具有显著的促进作用,具有广泛的普适性以及巨大的临床转化潜力。
此项工作是李子福教授课题组在力学赋能纳米药物抗肿瘤作用方向的又一重要研究成果。李子福教授课题组长期从事RES-blockade策略增强纳米药物抗肿瘤作用以及纳米凝胶的制备与表征相关研究。2018年至今,李子福教授课题组在Nature Communications,Nano Today,Advanced Science,Nano Letters,Biomaterials,Journal of Controlled Release等国际权威期刊上发表了一系列研究论文,系统阐释纳米凝胶理化性质的调控以及RES-blockade策略在纳米药物递送中的作用。本研究是前期工作的综合应用,阐明了基于硬质纳米凝胶的RES-blockade策略对纳米药物抗肿瘤的增效作用。
华中科技大学生命学院博士生李峥为该文章的第一作者。生命学院李子福教授为该工作的通讯作者。该论文得到国家重点研发计划项目、国家自然科学基金、以及华中科技大学学术前沿青年团队(生物力纳米肿瘤学)等项目的资助。
论文链接:https://doi.org/10.1038/s41467-023-37150-3